Oorzaak
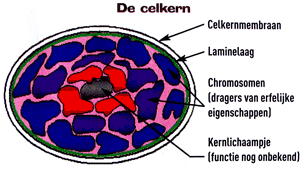
De speurtocht naar de genetische variatie die de versnelde veroudering bij deze kinderen veroorzaakt, was als zoeken naar een speld in een hooiberg. Het menselijk genoom kent drie miljard basenparen die in principe een rol kunnen spelen bij een ziekte. Ondanks dit onvoorstelbare getal is er de laatste decennia veel vooruitgang geboekt in de moleculaire ontrafeling van genetische aandoeningen.In 2003 ontdekte een Franse arts, Dr. Nicolas Levy, op het DNA van een progeriapatiëntje de plaats van een genetisch defect. Dit 'foutje' treedt waarschijnlijk spontaan op bij één van de eerste celdelingen na de conceptie. Kort na deze ontdekking werd de bevinding van Dr. Levy nog eens bevestigd door Amerikaanse onderzoekers.Het gaat om een eenmalige, spontaan voorkomende verandering van een erfelijke factor; een mutatie. Het is echter niet het gen zelf dat de aandoening veroorzaakt, maar wel het slecht of niet werkende eiwit waarvoor dat gen de code levert. De wijziging in de genetische code leidt ertoe dat de structuur van het eiwit verandert en het zijn functie verliest. De werking van het eiwit verandert. Er wordt niet de juiste hoeveelheid eiwit aangemaakt of de hoeveelheid eiwit is onaangepast aan de op dat ogenblik heersende fysiologische omstandigheden in de cel. Bij het ontstaan van deze ziekte is het eiwit de boosdoener. De genetische fout op DNA-niveau is heel basaal, maar het is wetenschappers inmiddels wel gelukt om die op te sporen.De mutatie die Progeria veroorzaakt zit in de drager van de erfelijke eigenschappen in de celkern: het gen. Het gen dat 'codeert' voor het eiwit Lamine A is bij deze ziekte beschadigd. Lamine A is een proteïne. Proteïne (nodig voor zeer ingewikkelde verbindingen van stikstof, koolstof, zuurstof en waterstof, soms ook zwavel of fosfor) houdt de celkern samen, zorgt ervoor dat de cel haar werk kan doen en zich kan reproduceren.Door de afwijking aan het LMNA-gen kan het lichaam van Progeria-patiënten het eiwit aan de binnenkant van de kern van delende cellen niet goed samenstellen. Dit heeft grote gevolgen voor het functioneren en de levenskracht van die cellen.Lamines zijn dus onmisbare stoffen. Normaliter zorgt het LMNA-gen voor de productie van twee eiwitten (Lamine A en Lamine C) die de binnenkant van de celkern vormen. Deze Laminelaag beïnvloedt de activiteit van de cel. Bij een beschadiging van het gen kan de cel niet goed functioneren.
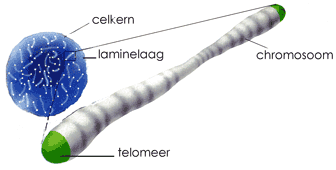
In het binnenste van de Progeriacel blijkt dat op de chromosomen de eindsecties ook sterk verkort zijn, wat een duidelijke indicatie is voor de beperkte levenskracht van cellen.
Men ziet in het oplossen van het raadsel Progeria ook wel eens de sleutel tot onsterfelijkheid. Sommige wetenschappers geloven namelijk in het bestaan van een soort levensklok in iedere celkern. Hun bevindingen wijzen erop dat de eindsecties van de chromosomen (de telomeren) een dergelijke klok bevatten. Bij gezonde mensen worden bij elke celdeling zo’n 50 bouwsteentjes van het DNA opgebruikt. Het levenselixer van een normale cel is dan pas na 80 tot 100 celdelingen verdwenen. Zonder telomeren sterft de cel. Volgens deze theorie beperkt dit ons leven tot maximaal 120 jaar. Bij kinderen met Progeria zijn de telomeren 8 keer sneller opgebruikt en kan het verval van het lichaam niet worden tegengegaan.Door de manier waarop de cellen met de verbranding omgaan wordt zuurstof verbruikt en energie opgewekt. Dit heeft veroudering tot gevolg. Bij dit proces komen op oudere leeftijd in toenemende mate zogenaamde zuurstofradicalen vrij die erg reactief zijn en de cel beschadigen. Als gevolg daarvan stokt de productie van verschillende hormonen en ontstaat een tekort aan noodzakelijke bouwstenen voor de renovatie. Dit veroorzaakt ouderdomsaandoeningen als immuundefecten en artherosclerose. Cellen die zijn vernietigd door de zogenaamde ‘vrije radicalen’ kunnen niet meer regenereren of vervangen worden.
De mutatie die het Hutchinson-Gilford syndroom veroorzaakt ontstaat bij toeval. Het vermoeden bestaat dat er naast LMNA ook andere genen bij het ontstaan van de ziekte betrokken zijn. Men heeft inmiddels een test ontwikkeld om de ziekte Progeria op jonge leeftijd te kunnen diagnostiseren. Zelfs een prenatale test is nu mogelijk, maar dat wordt gezien de zeldzaamheid van de ziekte nauwelijks toegepast.
Soms wordt HGPS ook vergeleken met een andere verouderingsziekte: het Werner-syndroom. Maar er zijn veel verschillen. 'Werner' is erfelijk, en in tegenstelling tot Progeria ontstaan er bij deze aandoening ook ouderdomskwalen als staar of diabetes. Bij Wernerpatiënten openbaart de ziekte zich pas na de pubertijd, of zelfs op volwassen leeftijd. Gemiddeld worden zij ongeveer 40 jaar oud.
De diversiteit aan ouderdomsziekten maakt duidelijk dat er bij veroudering veel genen zijn betrokken. Langzaam maar zeker groeit door het onderzoek naar deze ziekten ook het inzicht in normale verouderingprocessen. |
Veroudering kent vele aspecten. Progeriapatiënten komen dicht in de buurt van versnelde normale veroudering, maar niet in alle opzichten. Veroudering is voor delende cellen een ander fenomeen dan voor niet-delende cellen. Progeriapatiënten lijden in principe onder de veroudering van delende cellen.
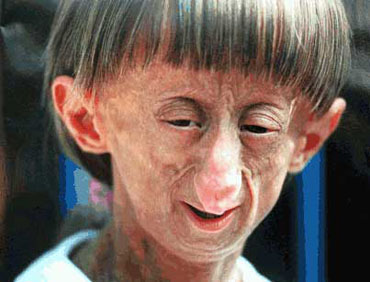
Omdat Progeria geen normaal verouderingsproces is, vertonen de kinderen ook niet alle kenmerken van veroudering: zo ontwikkelen zij een normale intelligentie en komt ook een ouderdomskwaal als dementie niet voor.
Soms wordt HGPS ook vergeleken met een andere verouderingsziekte: het Werner-syndroom. Maar er zijn veel verschillen. Deze aandoening is erfelijk, en in tegenstelling tot Progeria ontstaan er ook ouderdomskwalen als staar of diabetes. Bij Wernerpatiënten openbaart de ziekte zich pas na de pubertijd, of zelfs op volwassen leeftijd. Gemiddeld worden Wernerpatiënten ongeveer 40 jaar oud.
De diversiteit aan ouderdomsziekten maakt duidelijk dat er bij het verouderingsproces veel genen zijn betrokken.
normale huidcel
Progeria huidcel
deze foto's zijn beschikbaar gesteld door Dr. Leslie B. Gordon |